نوعية المياه المستخدمة يخضع للشروط نوع العملية والمعدات التكنولوجية. استخدام المياه المختلفة بالمصانع الكيميائية: نهر, الارتوازية, تمت تصفيتها, koagulirovannuû, برود, جزئيا أو كلياً obessolennuû, شرب إلخ.
يتم استخدام المياه العذبة الطبيعية دون المزيد من تنقية العمليات في الصناعة الكيميائية في تجهيز المواد الخام الأولية, منتجات التبريد والأجهزة والعمليات الفرعية المختلفة. وفي معظم الحالات، يتم معاملة المياه الطبيعية (القعود) تقنيات مختلفة تبعاً للطبيعة من الشوائب، ومتطلبات, المياه متطلبات بيانات الإنتاج.
تطبيق عملية معالجة المياه الميكانيكية, المادية, الطرق الكيميائية والفيزيائية-الكيميائية: دودج, تليين, التبادل الأيوني, أوبيسكريمنيفاني وجليحه. مياه الشرب, وبالإضافة إلى ذلك, تطهير. في الرسم التخطيطي أعلاه، (الشكل 16.1) التقنيات الأساسية لمياه الشرب..
إشراق المياه هو أساسا أساليب ترسب الشوائب, أطلق سراحه من المياه في شكل حماة. يتم استدعاء هذه الأساليب أيضا تنقية, أما بالنسبة لتحديد الشوائب في المياه حقن الكواشف الخاصة. عمليات الترسيب, تستخدم لتوضيح المياه, وتشمل تخثر, أوبيسكريمنيفاني ليمينغ والمغنسيوم.
تحت التخثر فهم العملية الفيزيائية-الكيميائية لالتصاق الجسيمات الغروية وتشكيل الجسيمات ميكروفاسي (فلوكول) منذ الترسيب ثم. الكواشف, يسمى تخثر, وعادة ما تطبق كبريتات Al.2(لذا4)3 و FeSO4.
تحسين تأثير تخثر الدم هو الذي تم التوصل إليه عند إضافة منتجات (بولياكريلاميدي, الحامض السليكى النشط، إلخ.). في حين تسريع تشكيل رقائق وتحسين هيكلها.
الذي تم إنشاؤه hlop′evidnuû الكثير, تتكون أساسا من هيدروكسيدات ال والحديد والشوائب, تخصيص المياه في الأحواض أو osvetlitelâh الخاصة (بقايا في لهم الدعم في وقف تدفق قادمة من الجزء السفلي من الماء), الضغط أو مرشحات مفتوحة والاتصال osvetlitelâh مع تحميل المواد الحبوب (رمل الكوارتز, سحقت انثراسايت, توسيع الطين, Šungizit، إلخ.), كذلك القشط, جيدروسيكلونة, مرشحات محبوكة. لإزالة جزئية الخشنة من الشوائب والعوالق النباتية, من الخزانات بلوم, تطبيق مش ميكروفيلتيرس, شبكة مسطحة وطبلة.
ليمينغ المياه تقليل المياه القلوية تحلية. وفي الوقت نفسه انخفاض صلابة, الملوحة, تركيزات شوائب الخشنة, مركبات الحديد وحمض السليكى.
كاشف لهذه العملية حي الليمون Ca(أوه)2, خدم كتعليق في المياه (حليب الجير). لتحسين كفاءة إزالة حمض السليكى في المياه إضافة الكاوية المغنسيت (من 70 إلى 80 % MgO).
هذه العمليات, وكقاعدة, جنبا إلى جنب، وتجري في نفس الوقت في جهاز واحد--أوسفيتليتيلي. التنظيف النهائي من الرواسب وتجري عملية التصفية باستخدام. اعتماداً على حجم الجسيمات لتتم تصفيته والجسيمات القطر المسامية الفعالة الاحتفاظ يمكن أن تحدث سواء في مدى طبقة الترشيح (لاصق الترابط وتصفية), وعلى سطحه (الترشيح الغشائي).
كما تصفية المواد أساسا استخدام رمال الكوارتز, سحقت انثراسايت, تنشيط الفحم الفحم, لب الورق, البيرليت, الخبث البركاني, توسيع الطين إلخ.
تسمى المياه Umâgčeniem إزالة مركبات الكالسيوم والمغنيسيوم, المساهمة في صلابة المياه. واحدة من الطرق الأكثر فعالية لتليين المياه هو الأسلوب الصودا الجير في تركيبة مع الفوسفاتية. تليين عملية تستند إلى ردود الفعل التالية:
1) تجهيز الجير حي لتصحيح صلابة مؤقتة, إزالة أيونات الحديد وملزم أول أكسيد الكربون2:
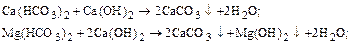
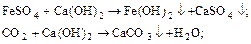
2) تجهيز الصودا كالتسينيروفانوج للقضاء على صلابة دائمة:
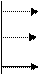
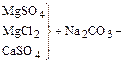
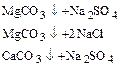
3) تجهيز تريناتريجفوسفاتوم لأكمل ترسب الكاتيونات Ca2+ و ملغ2+:
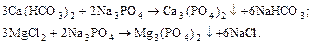
لا يكاد أن القابلية للذوبان الفوسفات الكالسيوم والمغنسيوم, يوفر الأسلوب الفوسفات عالية الأداء.
حاليا لتليين, obeskremnivaniâ تحلية المياه والطريقة المطبقة على نطاق واسع للتبادل الأيوني. وجوهرها, وهذا أيون صلبة مبادل يمتص اﻻلكتروﻻيت أيونات إيجابية أو سلبية مقابل مبلغ معادل للآخر, نفسه اتهم, أيونات. وفقا لعلامة على تبادل تهمة التمييز أيونات مبادلات الأيونات الموجبة وشاردة.
الأيونات الموجبة عمليا غير قابلة للذوبان في الماء المواد, تمثل ملح أو حمض الانيون, المساهمة في إينسولوبيليتي في الماء; الأيونات الموجبة نفس (أو هيدروجين الصوديوم) تتمكن من الانضمام إلى ظروف معينة في رد فعل تبادل الأيونات الموجبة الحل, فيه مبادل الأيونات الموجبة. الموجبة، على التوالي تسمى.33na-كاتيونيتامي وكاتيونيتامي ح.
قاعدة شاردة أو الملح مع الموجبة صلبة غير قابلة للذوبان. مبادلات شاردة تحتوي على مجموعة الهيدروكسيل منقولة (مبادلات يا شاردة).
غ-الأيونات الموجبة تستخدم سيليكات الألومنيوم: glauconite, زيوليت, بيرموتيت إلخ.; كالفحم أو المسلفنه أو الموجبة H, الراتنجات الاصطناعية; أنيونيتام يا راتنج الاصطناعية المركبة, على سبيل المثال، من اليوريا.
التبادل الأيوني بين الحل والمبادلات يتسم بطابع التفاعلات الكيميائية غير المتجانسة. وتجدر الإشارة إلى, تلك الشوائب, إزالة من الماء بطريقة التبادل الأيوني, ولا تشكل متسرعا, وأن هذا العلاج لا تتطلب جرعات مستمرة.
الخصائص هامة لقدرة التبادل الأيوني, يشير إلى قدرة سرير الراتنج على استيعاب كمية معينة من الأيونات في الظروف. تبادل القدرات يحدد مدة العمل دورة المرشحات إيونيتوفيه. عندما تصل إلى الحد المعين، تبادل أيون قدرة إجراء عملية الاسترداد (التبادل الأيوني, عقد بترتيب عكسي).
الشكل 16.2 مخطط الرقائق المياه مع التطبيق المتسق ل kationirovaniâ ح وأوه-أنيونيرو-بني. عند تمرير المياه من خلال مبادلات الأيونات الموجبة يتم إطلاق سراح من أيونات الكالسيوم والمغنيسيوم في تصفية ح-كاتيونيتوفوم 1, ومن ثم في تصفية شاردة 2 تتم إزالة الأنيونات من. ثم يمر الماء ديجاسير 3, حيث يتم تحريرها من الأوكسجين وثاني أكسيد الكربون, تواصل من خلال جمع 4 إلى المستهلك. لإعادة إنشاء عامل تصفية 1 تتيح للزوار مع حمض الكبريتيك, في عامل التصفية 2 --حل هيدروكسيد الصوديوم.
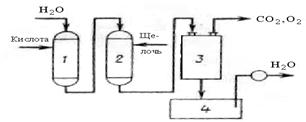
1 التصفية-كاتيونيتوفيج; 2 التصفية-أنيونيتوفيج;
3 -جليحه الجهاز; 4 --جمع المياه
الشكل 16.2 -الرسم التخطيطي لجهاز لتليين المياه
جزء هام من عملية تكنولوجية متكاملة المياه معالجة المياه-إزالة الغازات المذابة. وجود الغازات في المياه بسبب امتصاص وإفلاتها التفاعلات الكيميائية في تشكيل الشوائب في المياه الطبيعية, وظهور لهم خلال المراحل المختلفة للتنظيف. ويمكن تقسيم هذه الغازات إلى كيميائيا لا تتفاعل (ح2, O2, CH4) وتتفاعل كيميائيا مع الماء والشوائب، (NH3, CO2 Cl2), فضلا عن التآكل (O2, CO2, NH3, Cl2,ح2S) وخاملة (N2, ح2, CH4). تركيز غازات في المياه يتوقف على عوامل كثيرة; الرئيسية منها هي الطبيعة الفيزيائية للغاز, درجة التشبع, نظام ضغط ودرجة حرارة الماء.
الطريقة الرئيسية لإزالة الغازات الذائبة من المياه-الامتزاز (deaeration الحرارية). المبدأ إقامة اتصال مع بخار الماء, فيها الضغط الجزئي لغاز, المراد إزالتها من الماء, قريبة من الصفر, وهذا شرط ضروري للعملية من الامتزاز. تتم هذه العملية أساسا في deaèratorah (الفراغ, الغلاف الجوي, ضغط مستمر), وذلك عن طريق توزيع الماء والبخار تنقسم الحبر, الشريط وفقاعة. الفاصل الزمني للعمل نطاقات الضغط الفراغ من deaèratorah 0,0075 إلى 0,05 الآلام والكروب الذهنية.
وفي بعض الحالات، استخدام الطرق الكيميائية. لذا, لإزالة الأكسجين الموجود في المياه إضافة تأشيب قوية (على سبيل المثال, الصوديوم sulfite); إزالة ح2S تشلوريناتي المياه.
للحصول على المنتجات المكررة, اللازمة لإنتاج كواشف مختبر كيميائيا نقية, العقاقير الطبية, تحليلات مختلفة, تطبق في الممارسة المختبرية تحلية المياه الحرارية. تتم هذه العملية في مبخرات غلى نوع. إذا كان يتم إنتاج هذه المنتجات المكررة أساسا من المياه, خفف سابقا على مرشحات إيونيتوفيه.
أن الوجود في المياه من مسببات الأمراض والفيروسات يجعلها غير صالحة للاستهلاك المحلي, ووجودها في المياه لأنواع معينة من الكائنات الحية الدقيقة (على سبيل المثال, الخيطية, زوجليجنيه, بكتيريا سولفاتيريدوسينج, بكتيريا الحديد) أسباب الحشف, وفي بعض الأحيان تدمير خطوط الأنابيب والمعدات. تعقيم المياه ممارسة, وكقاعدة, معالجة بالكلور CL، سائلة أو غازية2, جيبوهلوريتامي ناكلو, Ca(ClO)2, ClO2. كما تستخدم لتطهير المياه والأوزون والإشعاع فوق البنفسجي.
تكاليف المياه والصرف الصحي التي تتراوح بين 5 إلى
15 % التكلفة للشركات الكيميائية.
الهواء في استخدام الصناعة الكيميائية, أساسا, كمواد خام أو ككاشف في العمليات التكنولوجية, فضلا عن أغراض الطاقة (مؤكسد الحصول على الطاقة الحرارية من خلال حرق أنواع الوقود المختلفة).
الهواء, يطبق ككاشف, يتعرض تبعاً لطبيعة إنتاج التنظيف الخاصة من الغبار, الرطوبة والسموم الاتصال. كما أنها تستخدم كسائل التبريد والمبردات في العمليات الصناعية. هواء مضغوط يستخدم على نطاق واسع في مختلف الحنفيات خلط محتدما سوائل وعجائن, في الطائرات-لرش السوائل في المفاعلات والمرافق.
الأكسجين النقي, ويفرز بواسطة تصحيح الهواء السائل, عادة ما تستخدم للأكسجين صهر المعادن, في عملية فرن لصهر المعادن، وما إلى ذلك..






