Поскольку давление насыщающего пара однозначно определяется температурой, а кипение жидкости наступает в тот момент, когда давление насыщающих паров этой жидкости равно внешнему давлению, температура кипения должна зависеть от внешнего давления. С помощью опытов легко показать, что при уменьшении внешнего давления температура кипения понижается, а при увеличении давления — повышается.
Кипение жидкости при пониженном давлении можно показать с помощью следующего опыта. В стакан наливают воду из водопровода и опускают в нее термометр. Стакан с водой помещают под стеклянный колпак вакуумной установки и включают насос. Когда давление под колпаком достаточно понизится, вода в стакане начинает кипеть. Так как на парообразование затрачивается энергия, то температура воды в стакане при кипении начинает понижаться, и при хорошей работе насоса вода наконец замерзает.
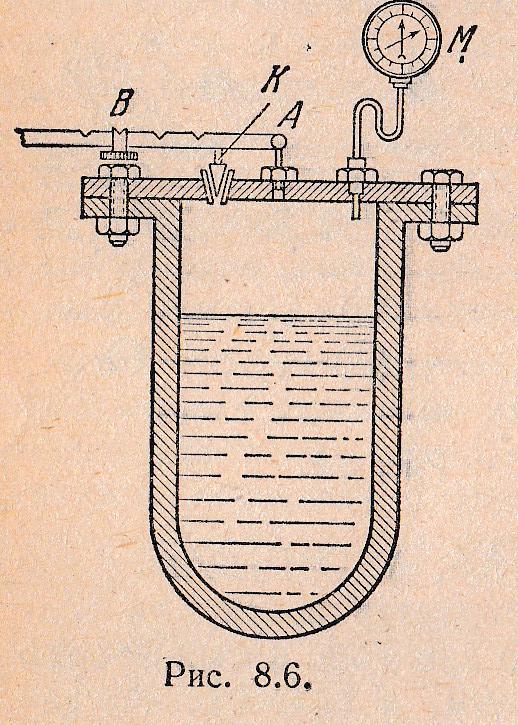
Нагревание воды до высоких температур осуществляют в котлах и автоклавах. Устройство автоклава показано на Рис. 8.6, где К—предохранительный клапан, АВ — рычаг, прижимающий клапан, М — манометр. При давлениях больше 100 атм воду нагревают до температуры выше 300°С.
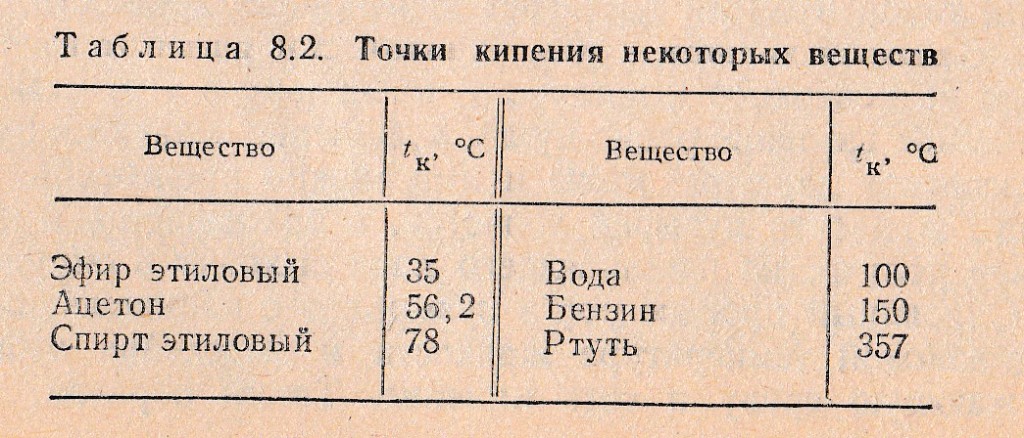
Температура кипения жидкости при нормальном атмосферном давлении называется точкой кипения. Из табл. 8.1 и 8.2 видно, что давление насыщающих паров для эфира, воды и спирта в точке кипения равно 1,013 *105-Па (1 атм).
Из изложенного выше следует, что в глубоких шахтах вода должна кипеть при температуре выше 100°С, а в горных местностях — ниже 100°С. Поскольку температура кипения воды зависит от высоты над уровнем моря, на шкале термометра вместо температуры можно указать ту высоту, на которой кипит вода при этой температуре. Определение высоты с помощью такого термометра называется гипсометрией.
 Опыт показывает, что температура кипения раствора всегда выше, чем температура кипения чистого растворителя, и возрастает при увеличении концентрации раствора. Однако температура паров над поверхностью кипящего раствора равна температуре кипения чистого растворителя. Поэтому для определения температуры кипения чистой жидкости термометр лучше помещать не в жидкость, а в пары над поверхностью кипящей жидкости.
Опыт показывает, что температура кипения раствора всегда выше, чем температура кипения чистого растворителя, и возрастает при увеличении концентрации раствора. Однако температура паров над поверхностью кипящего раствора равна температуре кипения чистого растворителя. Поэтому для определения температуры кипения чистой жидкости термометр лучше помещать не в жидкость, а в пары над поверхностью кипящей жидкости.
Процесс кипения тесно связан с наличием растворенного газа в жидкости. Если из жидкости удалить растворенный в ней газ, например, продолжительным кипячением, то можно нагревать эту жидкость до температуры, заметно превышающей температуру ее кипения. Такую жидкость называют перегретой. При отсутствии газовых пузырьков зарождению мельчайших пузырьков пара, которые могли бы стать центрами парообразования, препятствует лапласовское давление, которое при малом радиусе пузырька велико. Этим и объясняется перегрев жидкости. Когда она все же закипает, кипение происходит очень бурно.